فصل دوم
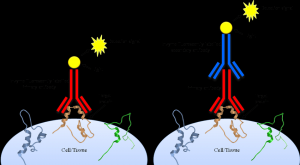
شناسایی اتو آنتی بادی های با استفاده از ایمونوفورسانس غیر مستقیم بر روی سلولهای HEP-2
شناسایی اتو آنتی بادی ها با استفاده از ایمونوفلورسانس غیر مستقیم بر روی سلولهای HEP-2
اتو آنتی بادی های خاص غیر اندامی (AABS) در برابر آنتی ژن های بسیار حفظ شده سلولهای خود بدن قرار می گیرند(۱۹۷۵ Holborow et al ) به لحاظ تشخیصی ساختارهای هدف مرتبط عمدتا در هسته ( آنتی بادی های ضد هسته ای ANA ) و همچنین در سیتوپلاسم قرار گرفته اند. غربالگری برای این AABS ها به منزله یک بخش عمده ای از روش های تشخیص برای بیماری های اتوایمنی کبدی و بافت پیوندی است . شواهد معمولا در چندین مرحله تشخیصی جمع آوری می شود که در آن غربالگری اولیه با استفاده از تست ایمونوفلورسانس غیر مستقیم IIF بر روی یک رده سلول ایپتلیال بوجود امده از سرطان حنجره در انسان یعنی سلول های HEP -2 انجام می شود. (۱۹۷۵ Hahon et al ) سلولهای HEP-2 جایگزین بخش های فریز شده اندام ها که در اصل بعنوان یک بستر استفاده می شدند ، می گردند . در غربالگری اولیه مزیت اصلی اصلی IIF (ایمونوفلورسانس غیر مستقیم ) بر روی سلول های HEP-2 این است که به لحاظ تشخیصی بررسی مناسبی بر روی ABBS های خاص غیر اندامی مرتبط و غلظت آنها فراهم می کند. در اصل آزمایشگاههای ایمنی سلولهای HEP-2 را خودشان تهیه می کنند . در کاربرد تشخیصی این سلولها بعلت شرایط تثیبیتشان و کشت خاص تنوع بسیاری دارند . امروزه آماده سازی با کیفیت مطلوب بوسیله تولید تجهیزات تشخیصی و اسلایدهای میکروسکوپی استاندارد بعنوان وسائل تشخیصی در محیط آزمایشگاهی در دسترس است(۱۹۹۸ EU Directive ) سلولهای مورد استفاده در IIF نمی توانند بوسیله سلولهای HEP-2 لیز شده بوسیله آنزیم ایمنی سنجی جایگزین شوند، زیرا تنها ایمونوفلورسانس قادر به رساندن اطلاعات تقریبا به همه AABS های مربوطه تشخیصی است . علی رغم آماده سازی HEP-2 در دسترس امروزی با کیفیت مطلوب برای ایمونوفلورسانس نتایج از آزمایشگاههای مختلف بطور قابل توجهی می تواند متفاوت باشد. بنابراین هدف این مقاله مطرح توصیه های مربوط به روش شناسی IIF و تفسیر الگوهای ایمونوفلورسانس بر روی سلول HEP-2 بطور خلاصه می باشد. این توصیه ها به بهبود مقایسه روشهای تشخیصی و کمک به تفسیر یافته های مستقل از آزمایشگاه که در آن آزمایش انجام می شود در نظر گرفته شده است . این توصیه ها با همکاری نزدیک دانشمندان بالینی و آزمایشگاهی و با تمرکز بر روی بهبود روش های تشخیصی بیماری های خود ایمنی توسعه داده شده است. (۲۰۰۷ Sack et al)
معرف ها و آماده کردن تست
سلولهای HEP-2
ازمنابع متعدد مورد تاییدی همچون FDA و CE و بانک های سلولی مانند مجموعه سلول وبافت آمریکا می توان سلول های HEP-2 را گرفت (WWW.atcc.org) شکل ، بیان آنتی ژن و تقسیم سلولی در این سلولهای ناهمگن است . سلولهای HEP-2 تغییر یافته نیز وجود دارند که در آنها بیان برخی آنتی ژن ها مانند Ro6 بوسیله ترانسفکشن افزایش یافته است . معیارهای خاصی برای تایید کیفیت سلول مهم هستند. کشت سلولی ، آماده سازی اسلاید میکروسکوپی ، تثبیت و دستورالعمل مراحل انجام به شدت بر روی فرآیند تولید اثر گذار است.
معیار ها عبارتند از :
- توزیع و تراکم سلول روی اسلاید میکروسکوپ
- تعداد میتوز (حداقل ۳ تا ۵ در میدان بینایی در بزرگنمایی ۲۰۰)
- بیان آنتی ژن های هدف برای اتوآنتی بادیهای مربوطه
- حفظ شکل
- پیش زمینه فلورسانس
تا کنون هیچ استانداردی برای تهیه سلولهای HEP-2 و یا ترکیب کیت های آزمایشی در بین تولید کنندگان نبوده است. هرچند این تضمین می کند که تفاوت ها در میزان تیتر و الگوهای فلورسانس مشخص شده بر روی ارزیابی نتایج مراحل آماده سازی اتفاق نمی افتد. علاوه بر این تنها روش های استاندارد ، مقایسه نتایج از آزمایشگاه های مختلف را ممکن می سازد . نظارت هر دسته نیازمند یک سرم منفی و حداقل سه نمونه سرم مثبت با الگوهای فلورسانس متفاوت در نتیجه واکنش آنتی بادی می باشد.(بعنوان مثال : سنترومر ،DNA دو رشته ای ،Ro.SSA ) این باید بطور متناوب هر بار که تست انجام می شود استفاده شود.
محل کار
آماده سازی تست های IIF و ارزیابی ثانویه بوسیله میکروسکوپ فلورسانس معمولا در فضاهای جداگانه انجام می شود . بسیار مهم است که در آزمایشگاههای ایمونوفلورسانس میزان گرد و غبار کم باشد. اتاق میکروسکوپ بایستی به اندازه کافی بزرگ باشد تا دونفر بطور همزمان بتوانند در آن کار کنند . در نظر گرفتن میزان گرما مهم است . مخصوصا زمانی که از میکروسکوپ هایی با لامپ جیوه فشار بالا استفاده می شود . بایستی یک شبکه ارتباطی برای کامپیوترهای آزمایشگاه در نظر گرفته شود تا مراحل کار و ذخیره اطلاعات به راحتی صورت گیرد.
روش انجام
تمام نمونه هایی که مورد بررسی قرار میگیرند در هر زمان با کمک مشخص کردن خصوصیات و برچسب زدن روی نمونه های قابل شناسایی و در دسترس هستند.
بررسی و پردازش نمونه ها
روش های پیش تحلیلی برای شناسایی اتوآنتی بادی ها مناسب نیست. همولیتیک ، لیپمیک ، و سرم مبتلا به زردی باید در پروتکل ثبت شوند، زیرا ممکن است سیستم آزمایش را تحت تاثیر قرار دهند . بعنوان یک قانون واکنشگرها باید دارای مجوز CE باشند. بنابراین آنالیز باید براساس دستور تولید کننده صورت گیرد.
هنگامیکه اسلاید میکروسکوپ بررسی می شود ، انحراف از انکوباسیون ، رقت و یا سیستم بافر می تواند نتایج آزمایش را تحت تاثیر قرار دهد . بنابراین باید تمام موارد در آزمایشگاه تایید شده باشند. نمونه های در اتاقی با دمای ۲۰-۲۴ سلسیوس بررسی می شوند. هنگامی که اسلایدهای میکروسکوپ از تولید کنندگان مختلف استفاده می شود لازم است اطمینان حاصل شود که اجزای آزمایش مربط در هر مورد استفاده شود. معمولا برای سوبسترای مربوط بر روی اسلاید میکروسکوپ سیستم های بافر و غلظت های جفت شدن تنظیم می شوند . همچنین آگاهی از تاریخ انقضا و روش های ذخیره ای مناسب برای هر واکنشگر مورد استفاده ، ضروری است . با جفت شدن یک کاهش خاص در غلظت انتظار می رود که می تواند به تیر پایین اتوآنتی بادی شود.
اسلایدهای میکروسکوپی تکرار شونده ،جایگاهی مورد استفاده ای در اندازه های مختلف دارند. لازم است که مطمئن شویم که کل جایگاه های مورد استفاده با سرم /جفت پر شوند. ما نباید اجازه دهیم که یک جایگاه مورد استفاده بیش از اندازه پر شود. زیرا باعث می شود سریعا جایگاه مورد استفاده بعدی در خطر آلودگی قرار گیرد . پیشنهاد می شود که هر آزمایشگاه حجم بهینه برای هر اسلاید میکروسکوپ را مشخص کند و این را در دستورالعمل وارد کند. برای جلوگیری از خشک شدن نمونه و کاهش حجم آن در هر جایگاه ، تک تک مراحل انکوباسیون باید در یک چاهک مرطوب انجام شود. جعبه های پلاستیکی صاف که براحتی شسته می شوند. برای این هدف به کار می روند. کف جعبه باید از مواد متخلخلی مانند سلولز که براحتی مرطوب می شود و قابل تعویض است ، پوشیده شود. نباید اسلایدهای میکروسکوپ بطور مستقیم در بالای این مواد قرار داده شوند. در واقع آزمایش زمانی شروع میشود که سرم با بافر مربوطه رقیق شده و به سلول HEP-2 تک لایه اضافه شود (معمولا بار فسفاته ایزوتونیک سالین ،PBS استفاده میشود.) تخت هیچ شرایطی نباید سرم بر روی صفحه های کناری ریخته شود. زمان انکوباسیون ۳۰ دقیقه است که بطور معمول بصورت سه تا ۱۰ دقیقه شستشو در PBS انجام می شود.(هر ۱۰ دقیقه یک شستشو با PBS انجام می شود.) زمانیکه از کورت استفاده میشود ، زمانی شستشو از ۲-۳ دقیقه تا ۵ دقیقه کاهش می یابد . استفاده از تجهیزات شستشوی اتوماتیک باید تنها بعد از ارزیابی جدی صورت گیرد ، زیرا گاهی به دلیل افزایش لکه ها و یا عدم چسبیدن سلولها نتایج راضی کننده نیست. وقتی اسلایده شسته می شوند پاک کردن تمام سرم ها یا ترکیب ها از سطح جایگاه بوسیله بافرهای مخصوص شستشو مهم است. این روش برای جلوگیری از تیتر بالای آنتی بادی و اشتیاق بالای آن به دیگر جایگاهها که منجر به آلودگی و نتایج مثبت کاذب می شود و همچنین در زمان هایی که انکوباسیون کوتاه است در نظر گرفته شده است .پس از اضافه کردن آنتی بادی ثانویه نشاندار شده با فلورسانس (جفت شونده) و انکوباسیون که معمولا ۳۰ دقیقه طول می کشد ، اسلاید دوباره شسته می شود. استفاده از آنتی بادی های ثانویه نشاندار شده با ایزوتیوسیانات فلورسانس (FICH) در IgG انسانی بسیار متداول است.
مزایای استفاده بیشتر از آنتی بادی های ثانویه در دیگر کلاسهای ایمونوگلوبین نیازمند تحقیقات بیشتر است . آنتی بادی های نشاندار شده با FITCH معمولا با ۰.۱ گرم بر ۱ لیتر اوانس بلو تیمار می شوند تا سیگنال فلورسانس راحت تر قابل تشخیص باشد. برای کامل شدن آزمایش اسلایدهای میکروسکوپ با محیط کشتی حاوی گلیسیرین (حدودا ۸۰ درصد گلیسیرین در PBS پوشیده می شود. این معمولا حاوی یک ماده ضد سفید کنندگی است. در هر آزمایش میزان ایده آل برای قرار دادن محیط کشت هر اسلاید میکروسکوپ باید ثابت باشد. هنگامی که اسلاید های میکروسکوپ بررسی می شوند، قرار گرفتن بیش از حد محیط کشت می تواند منجر به تیرگی و کاهش تمرکز گردد. تفاوت های خاص تولید کننده در قرار گرفتن محیط کشت باید در اینجا مورد بررسی قرار گیرد. عمل تمیز کردن و یا خشک کردن در اطراف سایت با حوله کاغذی یا سواب که در بعضی از آزمایشگاهها ابداع شده است غیر ضروری است و باعث پاک شدن مواد موجود در سلولها و تولید غبار و الیاف می گردد. ضربه زدن آرام به اسلایدهای میکروسکوپ و خشک کردن بر روی یک صفحه جاذب کافی می باشد. پس از ارزیابی ، اسلایدهای آماده شده را می توان در یخچال نگهداری کرد و تا ۲۴ ساعت تجزیه و تحلیل کرد . با این حال ، پس از دوره های طولانی ، تجزیه و تحلیل دوباره بعلت انتشار آنتی بادی ها و پاک شدن رنگ های فلورسانت دشواراست به ویژه هنگامی که واکنش پذیری دوباره ضعیف باشد. بنابراین اسلاید آماده باید محکم و کوچک بسته بندی شده و در دمای ۲۰ نگهداری شود. تجزیه و تحلیل ، نظارت و نقایسه لازم است بعدا انجام شود.
رقیق سازی سرم
در غبالگری آنتی بادی ها ، رقیق سازی سرم ۱.۸۰ صورت می گیرد . تعداد زیادی از کیت های آزمایش طراحی شده اند. ۹۵ درصد سرم های نمونه های کنترل سالم هیچ لکه ای نشان نداند در حالی که سرم های اتو آنتی بادی های مربوطه تشخیصی شناسایی شده اند.
معرف ها که بوسیله آزمایشگاههای جداگانه در کنار هم قرار داده شده اند(آزمایش های ساخته شده توسط آزمایشگاهها) باید در طول اعتبار سنجی تنظیم شوند در این رقت سرم منفی در خون اهدا کنندگان سالم ثبت نشده است . تولید کنندگان در اینجا باید با یک پروتوکل کلی موافقت کنند در مواردی مانند نتیجه مثبت آزمایش با استفاده از یکسری رقت های هندسی برحسب قدرت فلورسانس اولیه (۱:۶۰ تا ۱:۵۱۲۰) تکرار می شود.
تیترهای گرفته شده مرتبط تشخیصی حداقل در رقت ۱:۶۰ انجام شدن تست و ارزیابی در ست را فراهم می کند.(۲۰۰۴Kang et al) تیر ۱:۸۰ می تواند بعنوان یک مرز در نظر گرفته شود زیرا تعداد بسیار زیادی از نمونه ها با این تیتر ، مشخصه های مربوط به ANA غیر تشخیصی پیدا شدند.
کنترل-ها
به موازات پردازش نمونه ، تست های کنترل با نمونه های مثبت و منفی باید انجام شود. برای الگوهای مهم ، سرم های حاوی AABs معمولی نیز باید در فواصل منظم استفاده شود.
سرم های کنترل تجاری برای این منظور در دسترس هستند و پروب های مثبت تعریف شده توسط خود آزمایشگاه نیز می تواند مورد استفاده قرار گیرد از سرم های کنترل تعریف شده ایده آل از منابع تجاری و یا مرکز کنترل و پیشگیری از بیماری CDC باید استفاده شود.
میکروسکوپی
ارزیابی دقیق الگوها در بزرگ نمایی ۴۰۰ صورت گرفته است (ترکیب چشمی x10 وعدسی x40) . در ابتدا شدت فلورسانس مورد بررسی قرار می گیرد . ارزیابی می تواند با توجه به تعداد میتوزها انجام شود و تصمیم واضحی برای حضور و عدم حضور فلورسانس با توجه به الگوی اصلی گرفت . روشنایی نباید کمتر از لامپ بخار جیوه ۵۰ وات باشد. امروزه دیودهای منتشر کننده نور (LEDS) به میزان زیادی در منابع نوری بکار می روند. روشنایی ثابت و طول عمر آنها باعث شده است که جایگزین مناسبی برای لامپ بخار جیوه باشند(۱۰۰ تا ۳۰۰ ساعت)استفاده بسته به نوع آن ، تنظیم دوباره زمانی که لامپ تعویض می شود لازم است. تلاش برای استاندارد کردن فلورسانس هنوز موفق نبوده است . رویکرد هایی مانند استفاده از فیلتر های خاکستری مشخص ، رشته های فلورسانت استاندارد شده (۲۰۰۶ Kahn et al ) یا برنامه های کمکی تجزیه و تحلیل تصویر کامپیوتر محور Sack et al 2009 2007 Hiemann et al 2007 Soda 2003 در حال حاضر ارزیابی می شوند.
سلولهای HEP2 دارای طیف وسیعی از اتو آنتی ژنهای قابل تشخیص هستند. اولویت توجه به سمت الگوهای هسته ای است اما الگوی سیتوپلاسمی نیز باید در نظر گرفته شود. الگوهای ترکیبی متداول هستند . الگوهای جداگانه باید بصورت اختصاصی و در صورت مناسب بودن همراه با جزئیات تیترهای مختلف گزارش شوند. الگوهای مشخص در IIF بیماری مرتبط با AAB اختصاصی را نشان می دهد و این شاخصی برای استفاده از روش های ایمنی سنجی خاص است.
اختصاصی را نشان می دهد و این شاخصی برای استفاده از روشهای ایمنی سنجی خاص است . بنابراین در فرایند تشخیصی چند مرحله ای موثر، ضروری است که اتو آنتی بادی هایی که بطور معمول برای یک مرحله خاص پاسخگو هستند، مشخص شوند. برای محققان و پزشکان بایستی الگوهای فلورسانس که خصوصیات دقیق آنها مشخص نیست و آنهایی که ارتباط بالینی ناشناخته دارند مشخص شوند(۲۰۰۸ Fritzler) . آنتی بادی های ضد هسته ای به الگوهای اصلی کمی تقسیم می شوند این الگوها اغلب بعنوان الگوهای ترکیبی ارائه می شوند. این ها را می توان از راه مشاهده های مختلف در رقت های مختلف دید . برای مثال یک فلورسانس همگن قوی می تواند الگوهای دیگر را در رقت های پایین سرم مخفی کند و بنابراین آنها را بپوشاند . با توجه به تشخیص های مشکوک ، توجه به الگوهای فلورسانس که در شکل یک ذکر شده اند مفید است . این ارزیابی باید توسط کاربرانی با تجربه که بطور منظم بیشترین آموزش ها را در روش های تشخیصی اتوایمیون دیده اند، انجام شوند. تلاش زیادی با استفاده از کمک های تفسیری کامپیوتر محور صورت می گیرد(۲۰۰۷ Hiemann et al ، ۲۰۰۶ Kahn et al با توجه به سولات تشخیصی مطرح شده ، خصوصیات مشخص مورد نیاز است. برای تشخیص های متفاوت ، غربالگری باید بوسیله فرآیند های تشخیصی بر اساس روش های ایمنی سنجی اختصاصی (رادیو ، آنزیم یا ایمنی سنجی نقطه / خط )و یا استفاده گسترده از اتوآنتی ژنهای خالص سازی شده (طبیعی یا نوترکیب ) صورت گیرد. گزارش تشخیصی باید شامل آنتی ژن های هدف احتمالی و همچنین الگوهای فلورسانس و تیتر آنها باشد. مهمتراز همه گزارش باید حاوی یک ارزیابی باشد این امر بویژه برای نتایج منفی انجام می شود. از آنجا که در بیماران مسن آنتی بادی ها با تیتر اغلب نشانه ای از اختلال نیست . تیتر های مختلف می تواند نشانه های کلینیکی بودن یا نبودن آنها را حذف کند. گزارش یافته ها با ANA مثبت که متداول است بدون دادن جزیئات کافی نیست.
C پلومرفیک(PCNA) : رنگ آمیزی هسته ای پلی مرفیک و مرتبط با چرخه سلولی ، از همگن هسته ای به گرانولی که خوب یا ضخیم است.
D خالدار خوب: هسته خالدار خوب در اینتر فاز سلولها ، بدون هیچ نشان هسته ای
E خال درشت: نوکلئوپلاسمیک خالدار درشت ، بدون نشان هسته ای
F سانترومر : رنگ آمیزی نوکلئوپلاسمیک خالدار جداگانه در اینتر فاز سلولها ، نقاط سانترومری قوی نشاندار در صفحه متافاز
G هسته ای: رنگ امیزی همگن قوی معمولا با رنگ آمیزی همگن ضعیف نوکلئوپلاسمیک
H نقاط هسته ای : نئوپلاسمیک خالدار قوی ، آنتی ژن ۱۰۰ SP
خلاصه
شناسایی اتوآنتی بادی ها فاکتور مهمی در تشخیص و شناسایی بیماری های پیشرونده در بیمارانی با بیماری های خود ایمنی است. در تست های تشخیصی آزمایشگاهی برای بافت همبند و بیماری های خود ایمنی کبد ، ایمونوفلورسانس غیر مستقیم سلول های HEP-2 نقش اصلی در فرایند های تشخیصی چند مرحله ای دارد. علی رغم کیفیت بالای تشخیصی ، یافته ها در آزمایشگاه های مختلف بعلت نبود استانداردهاو همچنین فاکتور های درونی ، می تواند بطور قابل توجهی متفاوت باشد. این مقاله خلاصه ای از پیشنهادات برای فرایند استانداردسازی و تفسیر تست سلول HEP-2 و شناسایی آنتی بادی های غیر اختصاصی (بویژه ضد هسته ای) را بیان می کند. همچنین ملزوماتی درباره تست های تشخیصی شناخته شده ، دستور العمل های آزمایشگاهی ، ارزیابی و توصیه هایی برای تفسیر آورده است . برای فرآیند های تشخیصی آزمایشگاهی بهینه ، داشتن تشخیص کلینیکی دقیق مفید است. بعلاوه شاخص های کلیدی زیر پیشنهاد می شود:
غربالگری اولیه با استفاده از ایمونوفلورسانس غیر مستقیم بر روی سلولهای HEP-2 که با دقت انتخاب شده و با سرم ۱:۸۰ رقیق سازی شده اند.
ارزیابی زیر میکروسکوپ با روشنایی زیاد ، نتایج از تیتر ۱:۶۰ به بالا بعنوان مثبت در نظر گرفته می شود.
کنترل کیفیت آزمایشگاه و تفسیر استاندارد شده ها.
psoriasis
علت : پسوریازیس نوعی بیماری خودایمن ( پسوریازیس ، سندرم خستگی مزمن ، ام اس)ی و سیستمیک است که به نام بیماری صدف یا صدفک نیز شناخته میشود. در این بیماری تظاهرات پوستی بصورت پوسته ریزی فلسی ، خارش ، قرمزی و التهاب ، ضخامت پوستی و گاهی با تغییر رنگ پوست منطقه می باشد و در هر نقطه ای از بدن از سرتا پا و با گستردگی متفاوت و معمولا بعد از یک استرس شدید در بیمار نمایان یا تشدید می گردد.
بیماری پسوریازیس زاینده سه عامل است:
- عوامل محیطی (Environmental) که بسیار گسترده هستند و شامل آلاینده های محیطی ، آب آشامیدنی ، غذای فست فود ، مشروبات الکلی ، سیگار ، مواد مخدر ، گرده گیاهان و حتی طول و عرض جغرافیایی می باشند.
- عوامل عفونی (Infection) در بسیاری از موارد بیماری پسوریازیس بعد از عوامل عفونی ویروسی ، قارچی و باکتریایی خود را نشان می دهند که علت آن در دست تحقیق است.
- عوامل ژنتیکی (Genetics) پسوریازیس مانند بسیاری از بیماری ها ریشه ژنتیکی دارد و با HLA-cw6 میتوان آن را تشخیص داد لذا احتمال درگیری فرزندان بیمار پسوریازیس با ضریب ۲۵% وجود دارد.
از آنجایی که عوامل بسیار متعددی روی این بیماری موثر هستند بصورت ذاتی این بیماری گاهی بهتر و گاهی بدتر میشود.